1 はじめに

「痛み」はQOLを最も低下させる因子の一つです。がんに伴う痛み「がん性痛」はその代表の一つと言えます。痛みに耐えかねて、自殺を図ったり、安楽死を望んだり、そして安楽死を認めている国もあります。最近では痛みに関する研究や治療法が進歩し、がん性痛の治療も可能となっています。また、緩和医療と言う分野も確立されて、がん性痛の治療が主に行われます。
一口にがんといっても、全てのがん、全てのがん患者、がんの全ての経過に、同じような痛みが伴うわけではありません。がん性痛の「成り立ち」は一つでないからです(表1)。また、がん性痛治療は、ある程度の侵襲を伴ったり、機能・機質障害を余儀なくされたり、あらかじめ副作用を承知の上で行うものも少なからず有ります。しかし、これらを引き換えにしても痛みを取ることを優先したい、と言う場面は日常的に頻繁にあります。そこには、患者にとってはそれ程に耐え難い、家族にとっては人生の終末期を快適に過ごしてもらいたい、との複雑な背景があります。それゆえ、それぞれのがん患者の病状に合わせたがん性痛治療が必要となり、画一的なものは有りません。また、がん性痛に対処するには患者と家族、主治医が一体となって協力し合うことが重要です。
表1 がん性痛の成因と対処法
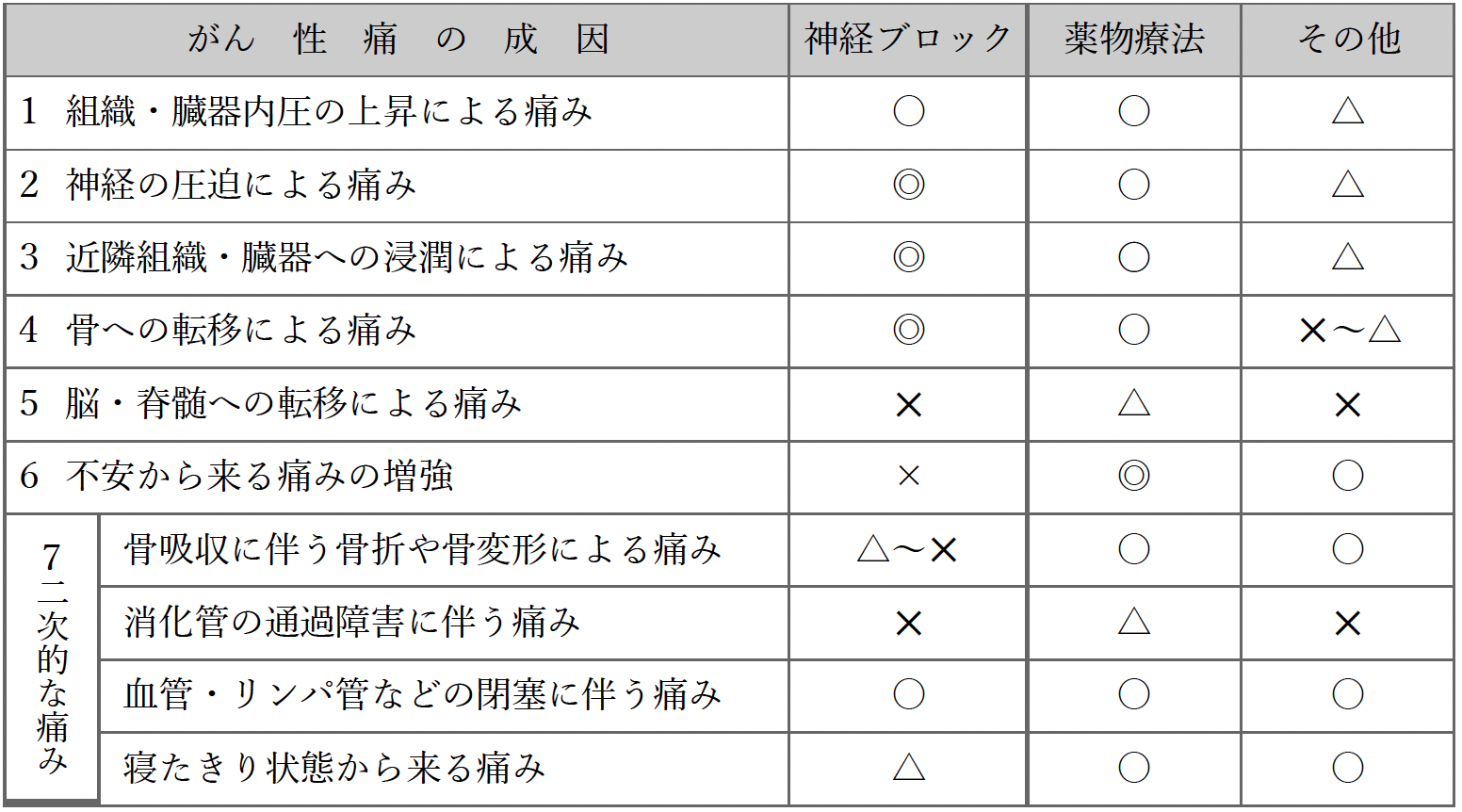
- 「神経ブロック」には、局所麻酔薬使用、神経破壊薬(高周波熱凝固を含む)使用によるものがあり、また硬膜外鎮痛法、経皮的コルドトミー、後根進入部破壊術や下垂体破壊術、脊髄刺激装置埋込み術も含まれる。
- 「その他」には理学療法(皮膚刺激法、運動療法、逆刺激療法、経皮的電気刺激療法、鍼療法など)や精神・心理・社会的療法(心理社会的介入法、リラクゼーション法とイメージ法、意識拡散法と再構成法、患者の教育、心埋療法と構造的支持、催眠術、精神面のカウンセリング、同病者支援グループなど)がある。
- これらは大まかな目安で、◎ 特に有効、○有効、△ 時に有効、× 無効または不適応。
2 がん性痛の成因と、対処法
がんそのものが痛みを発することは有りません。がん細胞の急速な増殖は、その組織・臓器、そして近隣組織・臓器への圧迫と浸潤などの影響を及ぼして痛みを発します。また、がんが転移すると、その組織・臓器で同じことが起こります。特にがんの病巣と神経組織が接近しているほど、痛みは強くなります。膵臓がんの痛みが強いのは、膵臓と腹腔神経叢とが隣り合っているからです。このようにがん性痛の原因は複雑です。しかもそれらが病状の経過とともに変化していきます。
がん性痛を軽減・消失させるには、基礎治療を行ってがん消滅あるいは縮小させることが、最も重要です。そのために、外科手術、化学(抗がん薬)療法、放射線治療などが不可欠です。これらの治療により痛みのコントロールが困難なときに、がん性痛治療が合わせて行われます。それには薬物療法、神経ブロック、手術などの方法があります。その他にも理学療法や精神・心理・社会的療法などもあります(ここでは紹介するのみに留めます)。
がん性痛の治療は、それぞれの痛みの成因に応じて表1のような基本的な治療が考えられます。これらを単独で、あるいは組み合わせて治療しますが、病状が伸展して末期に近づくにつれて体力が衰え、侵襲の強い治療は適応し難くなります。それゆえ画一的あるいは定型的ながん性痛治療はありません。このことはがん性痛の治療が非常に困難で、多岐にわたることを示しています。ここでは、医学的根拠が立証されている治療法を中心に説明します。
3 がん性痛治療を総合的に行うのが緩和ケア
WHOは、「生命を脅かす疾患による問題に直面している患者とその家族に対する介入」を緩和ケアと、2002年に定義しています。その代表ががん性痛の治療です。
- WHO方式がん性痛治療法
- がん性痛治療の基本が1986年にWHOから提唱され、1996年に改定されました。三段階に痛みを捉え(三段階除痛ラダー)、基本的に鎮痛薬と鎮痛補助薬の組み合わせた経口鎮痛薬を処方します(図1)。非ステロイド性消炎鎮痛薬(NSAID)から始め、痛みの強さに応じてオピオイド(モルヒネなど)や補助薬を組み合わせます。鎮痛の第一目標として「睡眠が痛みに妨げられない」、第二目標として「安静時には痛みを感じない」、第三目標として「体動時にも痛みを感じない」です。しかし、骨組織の痛みを体動時にも消失させ、神経障害に伴う自発痛を完全に消失させるには、しばしば困難を伴います。
この方式では、① 鎮痛薬の経口的投与、② 決まった時間に定期的投与、③ 三段階除痛ラダーに従って投与、④ 患者ごとの適切な投与量の選定、⑤ その上での細心の配慮、の5つの原則が示され、求められています。しかし「決まった時間に定期的投与」を例にとっても、夜間や外出時などの服用の煩わしさを否定できません。これを回避するため、長時間(12時間~24時間)作用性の製剤(徐放錠)が開発されています。
この様に、ある程度の改変も必要になります。内服薬の副作用には胃腸障害があり、これを回避するために経直腸投与(坐薬) や経皮投与(貼付薬)も含めても好いと考えます。がん末期の段階では、持続皮下注射、持続静脈内注射、持続硬膜外鎮痛法、さらには神経破壊や侵襲的治療法の考慮も必要になると思われます。一方、鎮痛補助薬の使用、神経ブロック、理学療法などは、どの段階でも行うのも可能です。
がん末期で体力が衰弱している場合、痛みが消失した途端に重篤な血圧低下(時には心停止)が起こり得るので注意が必要です。がん患者ではしばしば、貧血や悪液質が存在しますが、その一方では痛みによる極度の交感神経緊張状態が持続しています。このような交感神経過緊張状態は、貧血や悪液質による症状を覆い隠すことになります。そこに鎮痛が行われて過緊張状態が急激に解除されると、突発的な循環虚脱が起こり、ひどい場合は心停止に至ります。貧血や悪液質が疑われるときは、徐々に除痛を行う必要があります。それに交感神経の過緊張解除後は、気の弛みや疲労感が一気に顕在化して、病状が急激に悪化したかのように見えます。決してがん性痛の治療が病状を悪化させる訳ではありません。

(図1)
三段階の目標にしたがってオピオイド(モルヒネなど)を調節する。(第1目標)日中の痛みが軽減され、夜間よく眠れる、(第2目標)日中、安静にしていれば完全な徐痛が得られる、(第3目標)体重負荷時にも、体動時にも、痛みがない。そのために、比較的少量で投与を開始し、翌日その効果を判定し、痛みが残っていれば50%増量するという漸増法をとる。次第に増量していくと痛みが消失する量に達する。副作用、特に眠気があれば50%減量する。経口投与が原則である。基礎治療(放射線療法、化学療法)、鎮痛補助薬、神経ブロック、理学療法、などの治療はどの段階でも併用できると考える。
4 鎮痛薬
端的に言えば、「完全な除痛効果」をもたらすのは麻酔薬しかありません。完全な除痛下では手術が可能となります。そのような強力な薬剤を鎮痛目的で使用するのは極めて危険ですが、オピオイドとケタミンは、大量に使えば完全除痛が可能な麻酔薬としても使われますが、少量を用いれば鎮痛薬としても有用です。そのためには、安全域を超えてはなりません。
非オピオイド鎮痛薬と鎮痛補助薬の作用は、除痛ではなく、鎮痛効果と鎮痛補助効果ですので、大量使用したとしても。除痛・麻酔効果はありません(副作用として肝・腎機能障害や、血圧低下などが起こり、危険です)。主な鎮痛薬と鎮痛補助薬の一覧を表2に示します。
表2 がん性痛治療に用いられる鎮痛薬と鎮痛補助薬
| 種類 | 基本的薬剤 | 作用点 | |
|---|---|---|---|
| 非オピオイド | 非ステロイド性消炎鎮痛薬NSAID) | アスピリン、ロキソプロフェン、ジクロフェナクインドメタシン、ナプロキセン、など | COX-1、COX-2阻害 |
| エトドラク、セレコキシブ | COX-2阻害 | ||
| アセトアミノフェン | 脊髄内COX-2阻害、CD2受容体作動? | ||
| オピオイド | 弱オピオイド | トラマドール*、コデイン* | |
| 中オピオイド | ペチジン** | ||
| 強オピオイド | モルヒネ**、フェンタニル**、メサドン**、オキシコドン**、ブプレノルフィン*、ペンタゾシン*、タペンタドール** | オピオイド受容体作動 | |
| 鎮痛補助薬 | 抗うつ薬 | イミプラミン、アミトリプチン、など | MAOI |
| パロキセチン、フルボキサミン、セルトラリン、など | SSRI | ||
| サインバルタ、トレドミン、など | SNRI | ||
| 抗痙れん薬 | バルブロ酸、カルマバゼピン、など | Na+チャネル抑制 | |
| メマンチン、MK801、ケタミン**、など | NMDA拮抗薬 | ||
| ガプレガバリン、バペンチン、ミロガバリン | Ca2+チャネル・リガンド | ||
| バクロフェン、など | GABA受容体作動 | ||
| 抗不整脈薬 | リドカイン、メキシレチン、など | Na+チャネル遮断 | |
| 鎮静薬 | ジアゼパム、エチゾラム、など | GABA受容体活性化 | |
**は麻薬に指定されていない。** は麻薬に指定されている。
- 非オピオイド鎮痛薬
- アスピリンに起源を持つ薬剤を非ステロイド性消炎鎮痛薬(NSAID)といいます《グレードA》。プロスタグランジンを合成する酵素、COX-1とCOX-2を阻害することにより、炎症を抑え、また痛みの感受性を下げます。主な副作用の胃腸障害・腎機能障害の増強・喘息などは、COX-1の阻害に伴うもので、アスピリンは血液凝固機能障害を伴うことも有ります。最近では、COX-2を選択的に阻害するNSAIDが開発され、これらの副作用低下に役立っています。
かつてはアセトアミノフェンもNSAIDとされましたが、薬理作用が少なからず異なることから、別に分類されるようになりました《グレードA》。鎮痛作用はNSAIDに勝ります。しかし、その作用機序の詳細は不詳で、中枢神経系のCOX-2に作用する、カンナビノイド(CD2)受容体に作用する、などの学説が有ります。 - オピオイド 《グレードA》
- オピオイドにはμ作動薬、δ作動薬、κ作動薬の3種類があります。日常的にはμ作動薬(モルヒネ、フェンタニル、オキシコドン、ブプレノルフィン、トラマドールなど)、κ作動薬(エプタゾシン)、μ・κ作動薬(ペンタゾシン)などが用いられます。
μ作動薬には副作用が多く、吐き気、便秘、痒み、呼吸抑制、多幸感、排尿障害、依存症(いわゆる中毒)などがあります。これに比べれば、κ作動薬には目立った副作用は少ないようです。依存症に応じて麻薬指定されたものと、そうでないものが有ります。痛みのある患者にオピオイドを投与しても、依存症(中毒)は起りません(詳しい説明は省略)。これは、がん性痛治療にも当てはまりますので、オピオイド依存症を懸念する必要はありません。ペンタゾシンにはモルヒネなどとは異なった特有の依存症が認められ、これはμ受容体に加えて受容体(フェンサイクリジン受容体?)や他の酵素などへの作用と考えられます。
トラマドールは抗うつ薬の一つ(SNRI)として開発されましたが、臨床的に鎮痛作用が認められました。これは体内で代謝を受けて、モノ-O-脱メチル体(M1)に変化し、M1がμ作動薬として働きます。トラマドールとアセトアミノフェンを合剤にした内服薬もあり、広く使われています。
5 鎮痛補助薬
- 抗うつ薬 《グレードBときにA》
- 多くの抗うつ薬は、脳内のセロトニンやノルアドレナリン(まとめてモノアミン)の作用を増強します。モノアミンオキシダーゼ阻害薬(MAOI)や、特異的セロトニン再吸収阻害薬(SSRI)と特異的セロトニン・ノルアドレナリン再吸収阻害薬(SNRI)は抗うつ薬で、がんへの不安を和らげて精神状態を安定化作用を期待できます。その結果、がんによる抑うつ気分から解放され、痛みが和らぐ効果もあります。また、セロトニン性及びノルアドレナリン性下行性疼痛抑制系に作用して痛みを和らげるとの説もあります。副作用には眠気、ふらつき、眼圧上昇などがあります。
- 抗痙れん薬 《グレードA~BときにC1》
- プレガバリンなどは、神経シナプスのCa2+チャネルをブロックし、カルマバゼピン、フェニトインなどはNa+チャネルをブロックします。バクロフェンは中枢神経系のGABA受容体を作動して神経系の興奮を抑えます。NMDA拮抗薬(MK-807など)は興奮性のシナプス伝達を抑制します。これらは神経の伝導を妨げて痛みを和らげると考えられます。元々これらは抗痙れん薬として開発されました。
- 抗不整脈薬
- リドカイン、メキシレチンなどの抗不整脈薬は、Na+チャネルをブロックして神経の伝導を遮断し、痛みの感覚を減じると考えられます。
- 鎮静薬
- ベンゾジアゼピン系(ジアゼパム、エチゾラムなど)を始めとする鎮静薬は、脳内のGABA受容体のベンゾジアゼピン結合部位に結合して活性化させ、神経系を抑制することで鎮静作用を発揮します。この鎮静作用は、痛みを和らげると考えられています。
6 薬物療法の投与経路(注射によらない)
治療薬は色々ありますが、それぞれの痛み、その部位、進行状況、体力の状態、目標、などを考慮して、単独あるいは組み合わせで、安全かつ十分な効果を発揮する服用量を決定します。しかし、その効果を超えて突出する痛みが発作的に増強(突出痛)することがあります。これを抑えるために、その時々にオピオイドの内服や注射(レスキュー投与)を行って対処します。経口薬としてはオキシコドンやモルヒネ内服液などが用いられます(表3)。
表3 癌性疼痛治療の基本的な考え方
| 目標 | 留意点 |
|---|---|
| 社会復帰 | 運動傷害や膀胱直腸傷害を伴わない方法 カテーテルなどの留置は否 眠気、めまい、倦怠感などを伴わないことが望ましい 埋込み型脊髄刺激装置の適応、埋込み型注入ポートやポンプは可能 |
| 自宅療養(自立) | 運動麻痺や膀胱直腸傷害を伴わない方法 カテーテルなどの留置はない方が望ましい 埋込み型脊髄刺激装置の適応 埋込み型注入ポートやポンプは適応 |
| 自宅療養(介護) | 運動麻痺や膀胱直腸傷害を伴わない方が望ましい 持続皮下注射などのカテーテル留置はあってもよい 患者管理除痛法(PCA)は可 埋込み型脊髄刺激装置の適応 埋込み型注入ポートやポンプは適応 |
| 寝たきり(在宅) | 持続皮下注射などのカテーテル留置はあってもよい 患者管理除痛法(PCA)は可 埋込み型注入ポートやポンプは適応 |
| 寝たきり(入院) | 持続皮下注射 持続静脈内注射などのカテーテル留置はあってもよい 持続硬膜外鎮痛や患者管理除痛法(PCA)は可 埋込み型注入ポートやポンプは適応 |
| 終末期(意識あり) | 侵襲やリスクの高い治療法は避ける 侵襲の少ない薬物治療や神経ブロック・硬膜外オピオイドなどが適応 |
| 終末期(意識なし) | 基礎治療を優先する |
- 経口投与(錠剤、カプセル、散剤) 《グレードA》
- 経口薬の内服は最も簡単で、侵襲を伴いません。これは最も広く行われており、完全な終末期を除いて可能な方法です。初期~中期にはNSAID、そして中期~末期にはモルヒネなどのオピオイドが使用されます。
- 経直腸投与(坐剤) 《グレードA》
- 経直腸投与のための製剤(坐剤)があり、簡便に使用できますが、日本人には敬遠されがちです。大まかな特徴は、経口薬と類似していますが、胃腸障害が起こり易い人、経口投与が困難な人などに使用します。NSAID、ペンタゾシン、ブプレノルフィン、モルヒネなどの坐剤があります。
- 経皮投与(貼付剤) 《グレードA》
- 高濃度鎮痛薬を含んだパッチを皮膚に貼り付けるだけで長時間(1~3日間)安定して作用します。現在、フェンタニルやロキソプロフェンの調布剤が使用されています。非常に手軽ですが、皮膚は薬剤吸収が遅いので、調節性が乏しい、皮膚がかぶれる、などの欠点があります。
7 薬物療法の実際(注射や侵襲性のある)
注射や侵襲性のある鎮痛法も、効果や目的により多数存在します(表3)。
- 単回投与法 《グレードB》
- この方法は特別な器具や機器が不要ですが、安定した持続効果が得にくいのが欠点です。皮下注射、筋肉内注射、静脈内注射などの投与経路があります。
- 持続投与法 《グレードA》
- 携帯型持続注入ポンプを用いて、鎮痛薬を切れ目なく注入します。注入ポンプには鎮痛薬の注入速度とレスキュー投与量が設定できます。投与経路によって持続皮下注射や持続静脈内注射などが行えます。専用のプラスチック皮下針や静脈内針があり、主にモルヒネ、フェンタニルなどのオピオイドが使用されます。皮下注射であれば、短期間の在宅管理も可能です。静脈内注射は、通常は入院して行われ、長期化する場合は中心静脈カテーテルを挿入します。副作用は経口投与に準じます。
- 硬膜外鎮痛法 《グレードA》
- 鎮痛薬(主に水溶性の高いオピオイド)や局所麻酔薬を、持続注入ポンプを用いて脊髄硬膜外腔に投与する方法です。鎮痛薬を用いれば脊髄に直接作用して、運動機能を傷害せずに極めて強力な鎮痛効果を現します。局所麻酔薬を用いれば(持続硬膜外ブロック)、神経根や脊髄に作用して鎮痛効果を発揮します。μ作動薬を用いると、しばしば嘔気・嘔吐、排尿障害を伴います。κ作動薬のエプタゾシンは副作用が少なく、安定した効果があります。持続硬膜外オピオイド投与の副作用は経口投与に準じます。
硬膜外カテーテルを留置して、持続的に薬剤を注入し続けるのが持続硬膜外ブロックです。これは原則として嘔気・嘔吐を伴いませんが、ときに筋力低下、低血圧などを伴います。
持続カテーテルにより、まれに、硬膜外膿瘍や血腫を伴うのが欠点です。硬膜外カテーテルの留置には、原則として入院が必要で、専門医が挿入します。また、定期的なカテーテルの入れ替えが必要です。 - 患者管理除痛法(PCA) 《グレードA》
- 投与される鎮痛薬の量を患者自身でコントロールする方法で、そのための装置が開発されています。これを用いると、夜間でも患者自身の手でレスキュー投与が可能です。これにより患者は安心感が得られる、ナースを煩わす気兼ねが不要となる、などの利点があります。持続皮下・持続静脈内投与法や持続硬膜外鎮痛法に組み合わせて行います。薬物の乱用、過量投与を防ぐ装置が付いていて、安全です。
- 埋込み式注入ポート 《グレードA》
- 治療が長期にわたるときは、注入ポートや注入ポンプを皮下に埋込むことが出来ます。これにより、行動範囲が広がり入浴なども可能となるため、自立して社会復帰や自宅療養も可能となる場合もあります。また、注入ポートや注入ポンプの埋込手術は原則として入院が必要で、専門医が行います。
- 神経ブロック(薬剤による神経遮断) 《グレードA》
- 痛みの神経を局所麻酔薬で麻痺させるのが神経ブロックです。効果は一時的で、通常は毎週1~2回、繰り返し行う必要があります。知覚神経のみをブロックできる場合もありますが、多くの場合は運動神経もブロックするために、施行後は1時間程度の安静が必要です。硬膜外ブロックもこれに属します。
- 高周波熱凝固や神経は解約による神経ブロック 《グレードA》
- 特殊な専用の装置と注射針を用いた高周波熱凝固により、末梢神経、脊髄後根、後根進入部、脊髄背側路(経皮的コルドトミー)などの部位で、痛覚を脳に伝える神経をブロックことが可能です。神経破壊薬(アルコールやフェノール)を使用することもあります。これらによる神経ブロックは長期(数ヶ月~3年~それ以上)に及びます。いずれもメスを使うことなく低侵襲ですが、専門医により行われます。
神経破壊には痺れた感覚も伴います。ブロックした神経に運動神経が含まれていると、運動麻痺、筋力低下、膀胱直腸障害などを伴うことがあります。ブロックは一回で完遂できない場合が有り、複数回行うこともあります。
下垂体ブロックは鼻腔より下垂体に針を刺して下垂体を破壊する方法です《グレードB》。
これらには原則として入院が必要で、X線・CT・MRI・エコー透視下で、専門医が行います。 - 脊髄刺激療法 《グレードA~B》
- 痛みを感じている脊髄分節に相当する硬膜外腔に電極を挿入して(硬膜外ブロックと同じ方法で簡単に行える)、脊髄を電気刺激します。鎮痛効果には個人差があるので、試験的な脊髄刺激で効果が確認できれば、手術により刺激装置を皮下に埋込みます。運動神経の麻痺は起こらないので、社会復帰も可能という利点があります。神経には一切触れないので、障害が少ないですが、まれに刺激装置埋め込み部に血腫、感染、リンパ液の貯留、それに硬膜膿瘍を伴うことがあるのが欠点です。また、刺激装置の電池を交換する必要があります。
- 手術による神経遮断 《グレードB》
- 痛みを伝えている神経を目視下で破壊または切断します。末梢から順に、末梢神経切断術、脊髄後根切断術、後根進入部破壊術、脊髄背側路破壊術、脊髄交連切開術、下垂体切除術、などがありますが、現在はほとんど行われません。
8 おわりに
がん性痛治療は、このように様々な方法が考えられ、行われています。これは、完全かつ決定的な治療がないことを示しています。絶えず変化する病状と痛みに対し、適切な治療法を選択し組合せることが重要です。これには、患者とその家族、主治医の連携のみによって達成されます。
参考文献
- WHO編、がんの痛みからの解放第2版,金原出版,東京.1996.
- 日本緩和医療学会編,がん疼痛の薬物療法に関するガイドライン,金原出版,東京.2010.
- 日本癌治療学会編、がん診療ガイドライン,www.jsco-cpg.jp/guideline/23.html.
- 日本ペインクリニック学会編,慢性疼痛診療ガイドライン,信仰交易医書出版部,東京,2021.
- 日本緩和医療学会編,がんの痛み治療ガイド増補版.金原出版,東京,2017.
- 相田純久,硬膜外鎮痛法をκ作動薬とNMDA拮抗薬から考える.日本臨床麻酔学会誌,28: 204-216, 2008.
(2022.3.24 更新)